从解剖学角度来看,大脑可以被细分为多个特定区域,包括新皮层(neocortex)。大脑皮层是高级认知的中枢,是人类进化过程中大脑中扩张和多样化最多的区域。早期的大脑分区和皮层分区是由形态发生梯度(morphogenetic gradient)引导建立的,但随着发育进程的展开,这些早期模式如何产生更加精细更加离散的空间差异目前还不是很清楚。大脑皮层的发育过程已被研究了一个多世纪,历史上科学家通过每次只观察一种细胞类型,研究少量的基因,随后逐步拼接整个发育事件来进行探索。但我们必须意识到,大脑在同一时间并不是只产生一种细胞类型,而是数百种细胞类型一起发生发展,就像交响乐一样美妙且复杂。随着单细胞和空间转录组学的出现和发展,结合大数据分析,我们已经能够去探究神经发育这支交响乐中所隐藏的规律。
2021年10月6日,来自美国加州大学的Arnold R. Kriegstein团队在Nature杂志上在线发表了题为An atlas of cortical arealization identifies dynamic molecular signatures的研究论文。该研究利用单细胞测序研究了神经发育和早期胶质生成阶段10个主要的脑区和6个新皮层区域,揭示了不同皮层区域不同细胞纵向发育的分子图谱。
绘制人类大脑发育图谱为了描绘大脑发育过程中不同脑区及皮质区域的细胞多样性,作者收集了妊娠中期(怀孕3-6个月,神经发育高峰期)的大脑组织,随后进行为分割(大脑细分后的区域称为“regions”,皮层细分后的区域称为“areas”)和单细胞转录测序(图1)。作者从13个个体中拿到了10个脑区(主要是前脑、中脑和后脑)样本及6个新皮层区域样本(prefrontal cortex(PFC), motor, somatosensory, parietal, temporal 和primary visual(V1)皮层),最终获得了698,820个高质量的单细胞数据。通过UMPA(uniform manifold approximation and projection,新的降维技术,用于数据可视化和探索)分析,作者发现了预期的细胞类群(包括excitatory neurons,intermediate progenitor cells(IPCs),radial glia等)。数据表明,在整个大脑中,细胞类型是产生区域分化隔离的主要因素。区域特定基因分析显示,一些区域特异性基因存在于同一区域中的多个细胞类型中,说明某些区域性表达基因特征在细胞类型中具有高度渗透性。
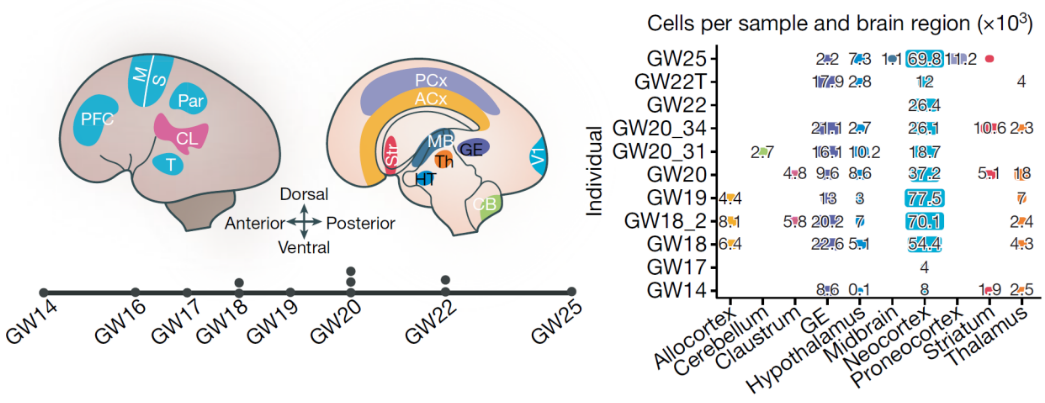
图1. 测序样本收集示意图
新皮质中的细胞类型已有研究表明新皮质包括几十个专门从事认知过程的功能区。V1和PFC中的神经元在出生后就完全不同,而其他的细胞类型并没有展示出明显的区域特异性差异。为了进一步扩展已有的研究,作者对来自于特定皮层区域的单细胞进行测序分析,获得了387,141个高质量的单细胞数据。通过分析,作者发现了预期的细胞类型,包括Cajal-Retzius neurons, dividing cells, excitatory neurons等。随后,按细胞类型进行分层聚类得到了138个新皮质细胞群,其中104个细胞群是由来自多个皮层区域的细胞组成的。
动态区域性基因特征为了探究新皮质发育过程中的细胞区域性差异,作者在皮质不同区域的兴奋性谱系中(radial glial (RG), IPCs和excitatory neurons)寻找每个细胞类型中的差异表达基因,同时通过检测已知的区域特异性基因的表达来评估皮质区域划分的可靠性。作者构建了星座图来探索不同皮质区域细胞类型之间的关系:RG节点主要在同细胞类型之间相互连接;IPC与兴奋神经元之间存在相互连接;PFC 和 V1 细胞类型节点之间没有连接,说明这两个基因表达模式之间相互排斥。在每一组区域标记基因中,作者鉴定了编码转录因子的基因,这些转录因子在特定区域的细胞中大量富集。其中包括一些在区域化过程中功能已知的转录因子,例如NR2F1和BCL11A,这两个基因都与神经发育疾病相关。作者还发现一些与皮层区域化不相关的转录因子:在V1中,包括NF1A, NF1B和NF1X,它们是大脑发育的重要调节因子,与大头症和认知障碍有关;ZBTB18, 大脑扩张驱动因子,与神经元分化和皮层迁移有关;在PFC中,包括HMGB2和HMGB3,它们在发育的不同阶段在神经干细胞中差异性表达,是神经分化的关键性调节因子,但它们在皮层区域化的过程中的功能未被研究和报道。
原位杂交验证候选标志物上述单细胞数据揭示了人类大脑发育过程中皮层的6个不同区域内细胞类型的多样性和转录谱。接下来,作者选择了兴奋神经元簇的候选标记基因进行验证,采用单分子荧光原位杂交(single-molecule fluorescent in situ hybridization, (smFISH))量化了20个样本中(来自4个皮质区域)31个RNA转录本的表达情况(图2)。与之前的报道一致,神经基因SATB2和BCL11B呈现区域动态性表达:他们在frontal区域共表达,但在occipital区域相互排斥。通过分析所有的区域,作者找到了新的亚细胞群标志物候选基因:NEFL, SERPINI1和NR4A1。这三个基因在PFC, somatosensory, temporal和V1皮层细胞中的表达量基本相等,但是它们相对的空间位置发生巨大改变:NEFL, SERPINI1和NR4A1在PFC中共表达,但在其他区域中相互排斥;在somatosensory皮层中,这些标记基因主要表达在上层分子层中。

图2. 自动化空间RNA转录检测流程
综上所述,该研究对新皮质区域不同细胞类型的基因表达特征提供了细致的理解。作者发现:(1) 在主要的大脑结构中,区域特征在不同的细胞类型中非常普遍;(2) 新皮质中的区域特征非常特殊,受限于单个细胞类型;(3) 除了细胞类型特征外,细胞的发育阶段(即妊娠周)是基因表达特征组合的有力决定因素。这些发现表明,区域特异性基因表达特征的动态变化速度非常快,而且是细胞类型特异性的(图3),这与之前的理论似乎不太一致,在以前认知中,基因表达模式通常被认为是一旦建立就会持续存在。通过绘制大脑发育过程中的基因表达图谱,研究人员对大脑皮层是如何形成有了更好的理解,有助于探索大脑皮层是如何在神经发育疾病中受到影响的。
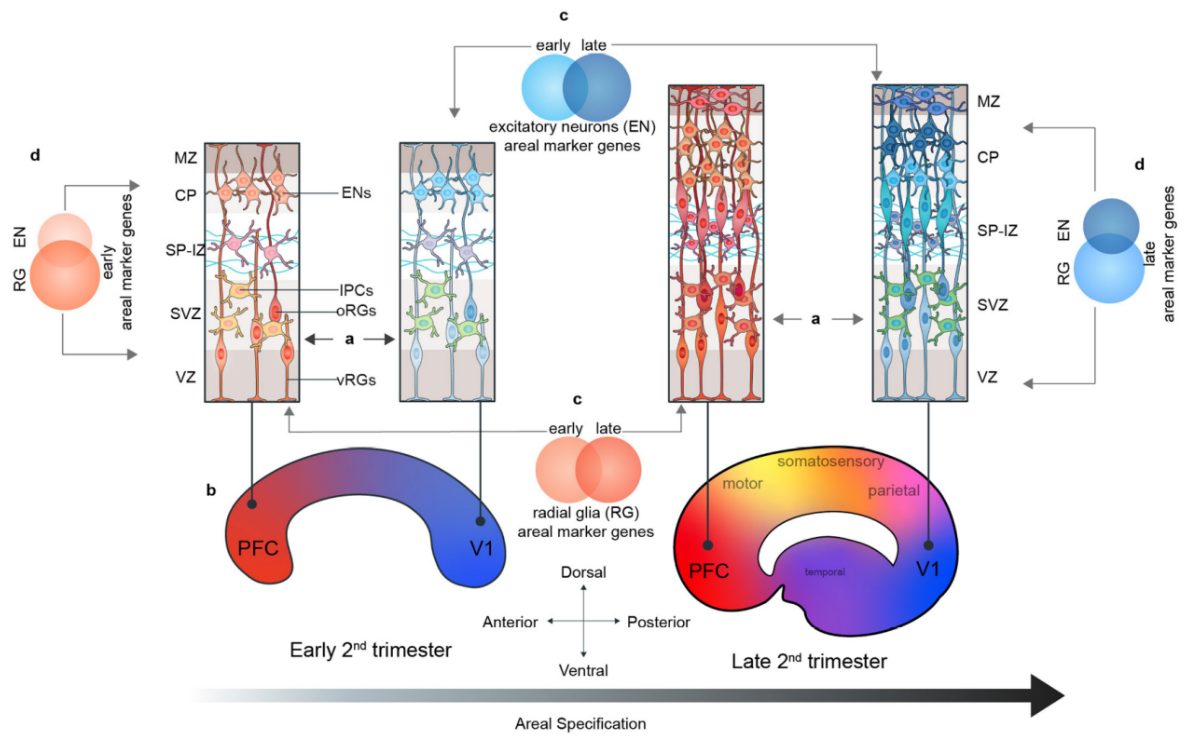
图3. 发育过程中皮层区域化模式图
原文链接:
https://doi.org/10.1038/s41586-021-03910-8
转自网络如有侵权请联系删除 !





